
摘要
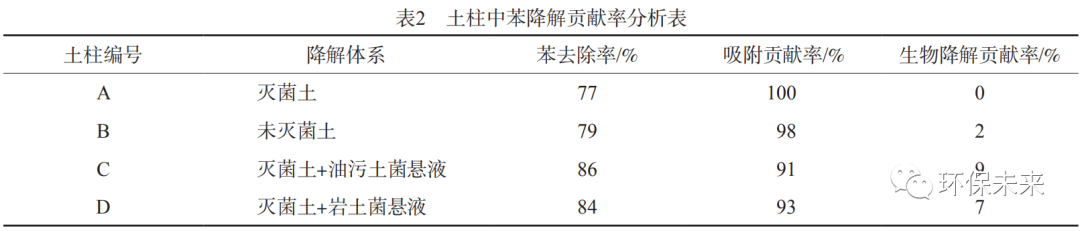
采用静水实验考察无菌和有菌条件下苯在不同埋深土壤中的自然降解规律,利用土柱实验探究天然和人工驯化微生物对苯的去除规律,并通过高通量测序识别优势菌群。实验结果表明:岩土菌悬液中的苯降解菌主要为红球菌属(Rhodococcus);油污土菌悬液中苯降解菌主要为假单胞菌属(Pseudomonas)。静水实验结果表明,微生物的存在可提高苯去除率,但土壤埋深越深,苯的去除效果越差。土柱实验结果表明:土壤对苯的吸附率约为77%,加入驯化微生物后,苯的去除率达到了84%~86%;天然微生物降解苯的贡献率仅为2%,驯化微生物的加入使微生物对苯降解的贡献率增大了3~4倍。
本工作通过静水实验分析了不同埋深的无菌和有菌土壤介质对苯的自然降解规律,并通过土柱实验探究天然和人工驯化微生物对苯的去除规律。为弄清微生物降解的潜力及生物强化修复的可行性,采取高通量测序手段分析微生物群落结构特征,为现场生物修复提供理论支撑。
1实验部分
1.1试剂、材料和仪器
苯:优级纯;HgCl2:分析纯。
微生物菌种:分别取齐鲁石化厂区附近200~300m深度处的灰岩及石油烃污染土壤(油污土)各200g,粉碎后用无菌去离子水浸泡24h,经0.2μm滤膜抽滤截留微生物,得到岩土菌种和油污土菌种。
实验土壤:采自厂区附近未受污染的可耕农田,取土深度为0.5,1.0,1.5m,分别记为浅层土、中层土、深层土。经风干、除杂、研碎后,过2mm筛。灭菌实验土壤:使用前将实验土壤在121℃灭菌锅中高温灭菌30min。
地下水:采自当地未受污染的地下水井,依据《地下水环境监测技术规范》(HJ164—2020)[13],经0.2μm滤膜过滤去除悬浮颗粒物,4℃保存。灭菌地下水:使用前将地下水在121℃灭菌锅中高温灭菌20min。
含苯渗流液:采用m(甲醇)∶m(灭菌地下水)=1∶100的甲醇-水溶液配制苯质量浓度为20mg/L的苯-甲醇-水溶液。
牛肉膏-蛋白胨液体培养基:牛肉膏3g,蛋白胨10g,NaCl5g,去离子水1000mL,~7.6。
无机盐培养基:Na2HPO44g,,NH4Cl1g,MgSO4·7,,FeSO4·7,,MnSO4·5,ZnSO4·7,CuSO4·5,CoCl2·6,去离子水1000mL,~7.6。
营养液:按微生物生长所需的营养元素比例m(C)∶m(N)∶m(P)=100∶10∶1配制,其成分包括葡萄糖、NH4Cl、K2HPO4、NaCl等。
HQ30D型水质分析仪:美国HACH公司;GI54TR型灭菌锅:美国ZEALWAY公司;AIRTECH型超净工作台:苏净安泰空气技术有限公司;6890N/5975B型气相色谱质谱仪:安捷伦科技公司;UV-6000PC型紫外-可见分光光度计:惠普公司;TGL型高速离心机:上海器械厂。
1.2实验方法
1.2.1苯降解菌的培养驯化
在两个500mL棕色广口瓶中分别加入岩土菌种和油污土菌种,再加入牛肉膏-蛋白胨液体培养基500mL,密封在(25±1)℃恒温条件下避光连续培养3d,分别得到岩土菌种子液和油污土菌种子液。
在两个1L的棕色微生物培养驯化瓶中各加入500mL无机盐培养基及作为唯一碳源的苯,再分别加入300mL岩土菌种子液和油污土菌种子液,于(28±1)℃恒温培养箱中连续培养[14]。7d后取1mL培养液测定苯质量浓度。剩余培养液在3000r/min下离心10min后去除上清液,将底部沉淀物转接至500mL新鲜无机盐培养基中,再次加入苯。重复上述过程,在驯化过程中逐步提高苯浓度,直到苯质量浓度从10mg/L提高至20mg/L。稳定培养2周,得到岩土菌悬液及油污土菌悬液。
1.2.2微生物降解苯的静水实验
分别取20g不同取样深度的实验土壤,置于100mL灭菌玻璃瓶内,加入含苯地下水溶液80mL,封口后15℃避光静置,各设置3组平行样。按相同方法设置无菌对照组:采用灭菌实验土壤,加入0.02mg/LHgCl2作为抑菌剂。分别在不同降解时间取样,每次抽取0.5mL上清液测定苯的质量浓度,并测定溶液的氧化还原电位(ORP)。
1.2.3垂直入渗条件下微生物降解苯的土柱实验
土柱实验装置示意见图1。有机玻璃柱(长30cm,内径5cm)用紫外灯灭菌30min。在柱内由下至上分别装填等质量的不同取土深度(1.5,1.0,0.5m)处的3种实验土壤,柱两端各装填1cm厚度的石英砂。
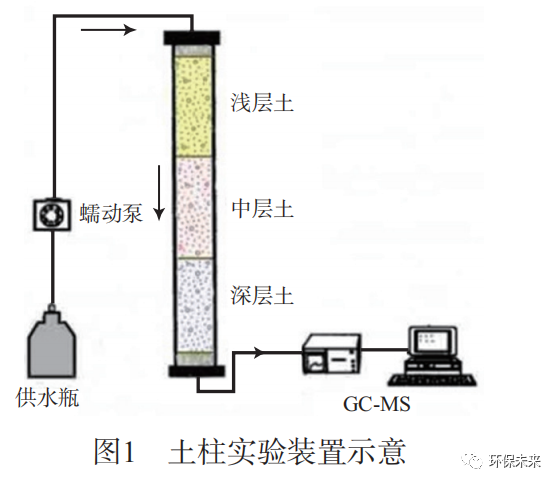
分别设计4组土柱实验(A,B,C,D组),每组各3个土柱作为平行样。A,C,D组中填充灭菌实验土壤,B组填充实验土壤。各土柱用无菌去离子水饱水24h后从柱顶通入含苯渗流液。其中A组的含苯渗流液中加入0.02mg/LHgCl2作为抑菌剂,B,C,D组加入营养液[15]。C和D两组分别缓慢注入10mL油污土菌悬液及岩土菌悬液。实验过程中维持流出液流量为5.2~5.5mL/h,定期收集并测定流出液中苯的质量浓度和ORP值。
1.3分析方法
苯质量浓度的测定采用气相色谱-质谱联用仪。色谱条件:DB-5毛细管柱;载气为He气,流量1mL/min,分离比5∶1;进样温度为250℃;升温程序起始温度为40℃,保持5min,以10℃/min的升温速率升至300℃,保持15min。质谱条件:EI电离源,能量70eV;离子源温度230℃,四极杆温度150℃,接口温度250℃,扫描范围30~500m/z。
驯化得到的苯降解菌的高通量测序委托上海美吉生物医药科技有限公司完成。
土壤有机质含量的测定采用重铬酸钾氧化-分光光度法(HJ615—2011)[16]。
溶液ORP的测定采用水质分析仪。
2结果与讨论
2.1苯降解菌的种类
通过高通量测序得到岩土和油污土菌悬液中微生物的丰度,见图2。由图2可见:从岩土中驯化出的苯降解菌主要来自不动杆菌属(Acinetobacter)、芽孢杆菌属(Bacillus)、黄杆菌属(Flavobacterium)、红球菌属(Rhodococcus)和假单胞菌属(Pseudomonas),其中红球菌属的微生物丰度最高;油污土菌悬液中包含了不动杆菌属(Acinetobacter)、红球菌属(Rhodococcus)和假单胞菌属(Pseudomonas)的微生物,其中假单胞菌属的微生物占有较高的丰度。有报道表明,假单胞杆菌和不动杆菌是环境中非常重要的两类降解菌[17]。
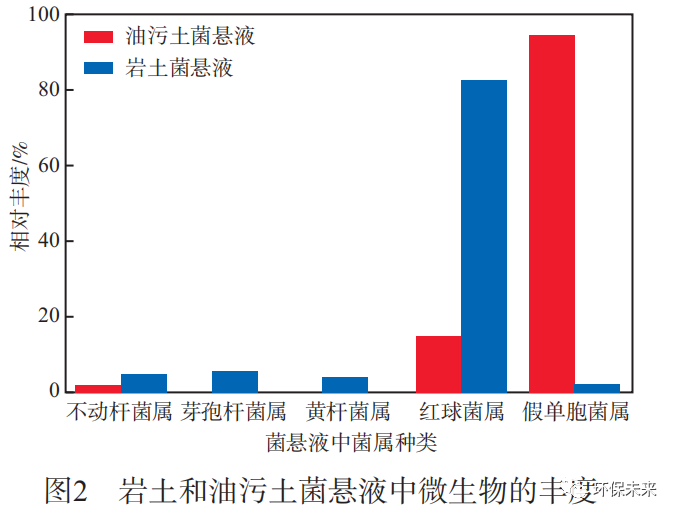
2.2静置条件下苯的降解效果
静水实验中苯质量浓度的变化见图3。由图3可见:实验运行的第1天,无菌和有菌条件下苯的质量浓度即出现明显差异,无菌条件下含不同深度实验土壤的地下水中的苯质量浓度从20mg/L降至10mg/L左右,而有菌条件下苯的质量浓度从20mg/L降到8mg/L左右;随着时间的延长,有菌和无菌条件下苯浓度降低趋势的差异更加显著,无菌条件下呈现轻微下降的趋势,而有菌条件下则显著降低,如无菌条件下浅层土中苯质量浓度在30d内由10mg/L仅降到9mg/L,而有菌条件下由8mg/L显著降低至2mg/L,这说明除吸附过程外,微生物对苯的去除起到了重要作用;有菌条件下浅层土、中层土、深层土的苯质量浓度在第30天分别为2.1,2.4,3.7mg/L,苯去除率分别为89%,88%,82%,较无菌环境下的苯去除率(53%,52.5%,50%)提高了约30百分点;并且埋深越深的土壤介质对水溶液中苯的去除率越低,呈负相关关系,原因可能是深层土中有机质含量相对较少,约为3.83%(表1),供给微生物生长的养分不足,使得微生物对苯的降解效果减弱[18]。
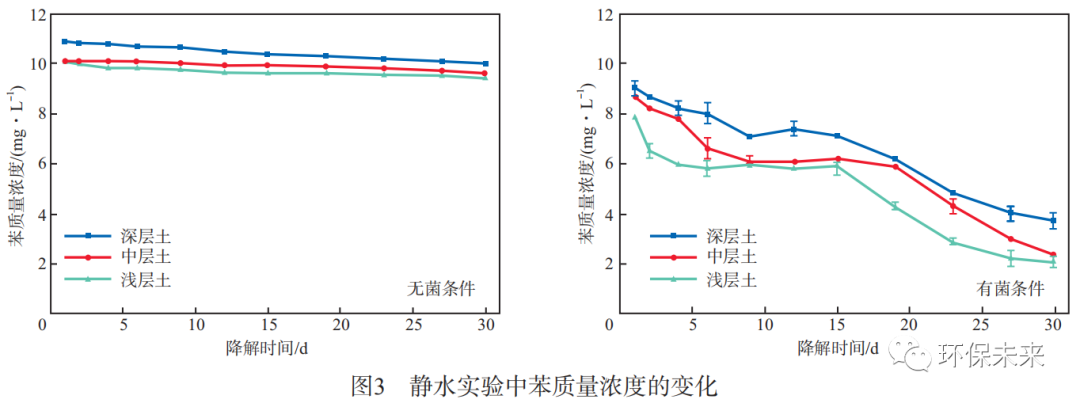
ORP可以反映出好氧微生物对石油烃的降解性能[19]。静水实验中ORP的变化见图4。由图4可见,无菌条件下反应液的ORP在30d内均维持在225mV左右;在有菌条件下,反应液的ORP有明显的下降趋势,第9天时ORP降低到200mV以下,最终维持在160mV左右。苯提供了充足的碳源,微生物降解苯的过程中消耗了溶解氧,ORP随之降低。但随着溶液中苯浓度的降低,生物降解速度变缓,ORP又逐渐趋于稳定[20]。
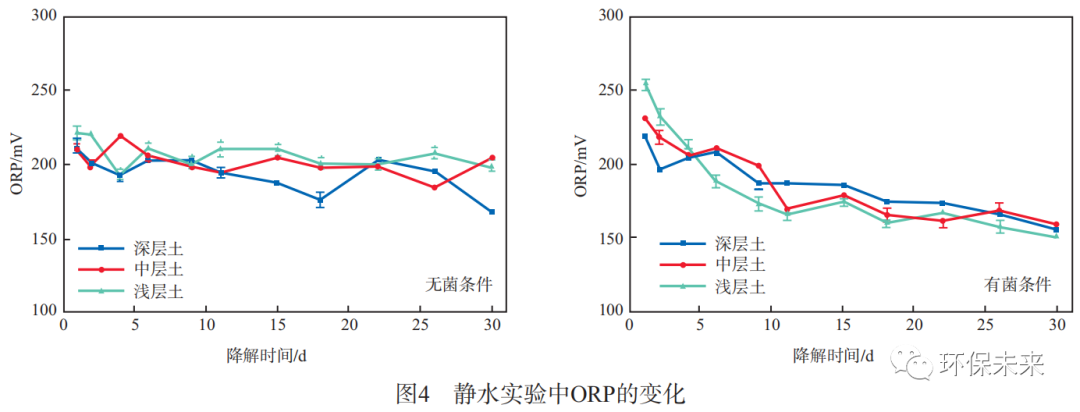
2.3垂直入渗条件下苯的降解效果
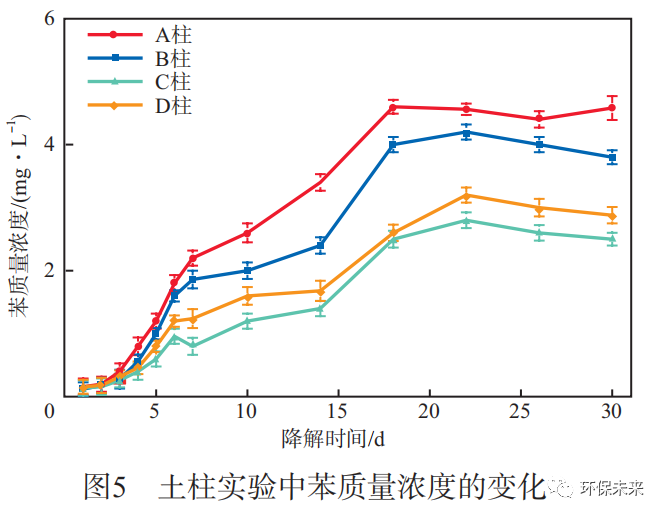
土柱实验中苯质量浓度的变化见图5。由图5可见:4个土柱流出液中苯的质量浓度均在18d后达到相对稳定;装有灭菌土的A柱主要是对苯的吸附效果进行研究,流出液中苯的质量浓度在第18天达到最高值,约为4.6mg/L,苯去除率为77%;含有微生物的B柱、C柱、D柱的流出液苯质量浓度均在第22天达到最高值,苯去除率为79%~86%。
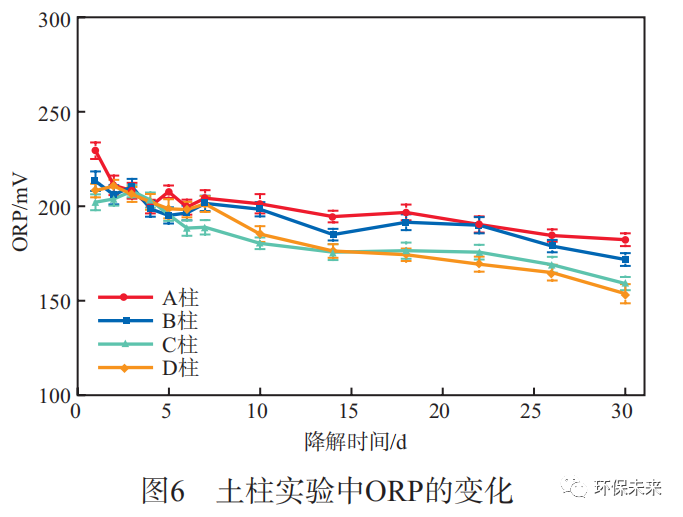
土柱实验中ORP的变化见图6。由图6可见:随降解时间的延长,ORP总体呈下降趋势;其中,加入驯化降解菌的C柱和D柱的流出液的ORP值均较低,最终维持在150~200mV,其原因是添加的微生物在生物降解过程中需消耗溶解氧,ORP随之降低,进而整个体系的氧化性降低。
3结论
a)含有微生物的土壤在30d内对地下水中苯的去除率可达到80%以上,较无菌环境下苯的去除率提高了30百分点。地下水中苯的去除率与土壤的埋深呈负相关关系。
b)进入含水层中的苯容易被土壤所吸附。在土柱渗流系统中,苯的吸附去除约占77%;吸附和天然微生物协同作用对苯的去除率约占79%;加入驯化微生物后,苯的去除率达到了84%~86%。
c)天然微生物对苯降解的贡献率约为2%。加入驯化微生物后,微生物的生物降解贡献率可提高3~4倍。其中,红球菌(Rhodococcussp.)和假单胞菌(Pseudomonassp.)等好氧菌是石油污染场地降解苯的主要微生物。
免责声明:以上内容转载自生态修复网,所发内容不代表本平台立场。
全国能源信息平台联系电话:,邮箱:hz@,地址:北京市朝阳区金台西路2社









