等温滴定量热法(ITC)是用于量化研究各种生物分子相互作用的一种技术,它可直接测量生物分子结合过程中释放或吸收的热量。通过测量结合过程中的热传递,就能够准确地确定结合常数(KD)、反应化学量(n)、焓(∆H)和熵(ΔS)。这就提供了有关分子相互作用的完整热力学信息。ITC是唯一能够在一次试验中同时确定所有结合参数的技术。ITC不仅可测定结合亲和力,还能阐明潜在分子相互作用的机制。ITC可以测定结合配偶体在自然状态下的亲和力,无需通过荧光标记或固定化技术对互作分子进行修饰。
一、测量原理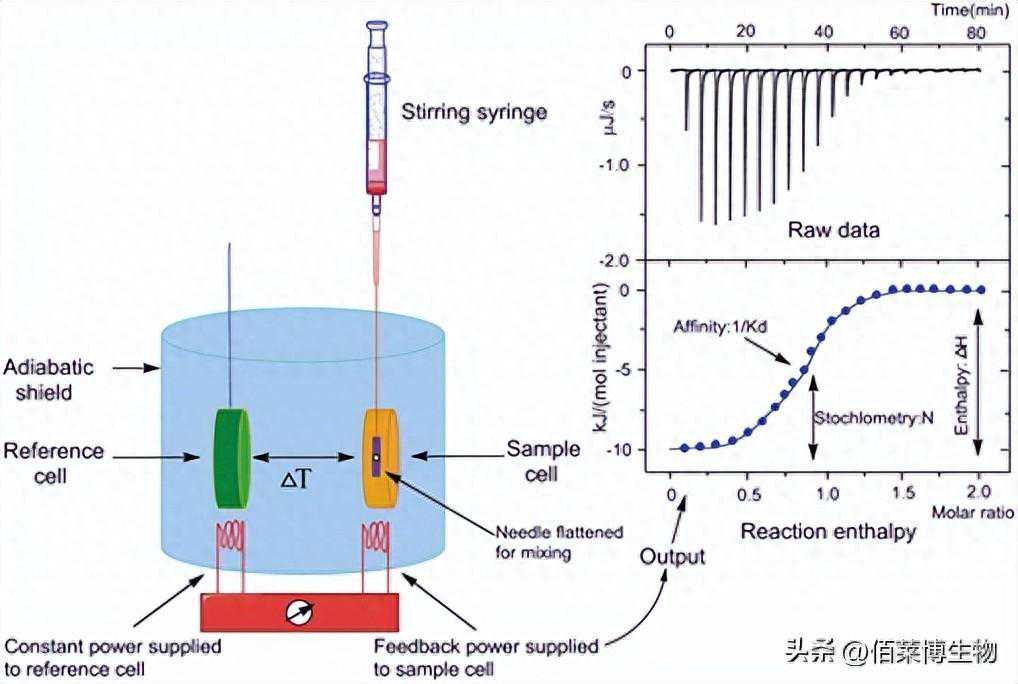
仪器包含一个参照池和一个样品池。参照池通常加入纯水,样品池加入待研究对象中的一种(一般为大分子,如蛋白质),而滴定器里则装有另一种研究对象称之为配体(例如化合物)。
在实验过程中,配体被可控地滴入样品池中(同时伴随充分混合),一般为0.5到2μL,直到样品池中的配体浓度2-3倍过量于样品池中的蛋白浓度。每次滴定会产生一个热量脉冲,通过对每一次滴定时热量的积分并对浓度进行归一化处理后生成摩尔放热量(kcal/mol)对摩尔比率(配体/样品)作图,再选择拟合合适的结合模型(BindingModels),获取结合相关的亲和力(KD)、化学结合计量比(n)、焓变(ΔH)和熵变(ΔS)。
二、测量过程参比池和样品池被设定到所需的实验温度。将配体装入一个非常精确的注射装置上的注射器中,将注射装置插入包含目标蛋白质的样品池中。将一系列小体积配体样品注入到蛋白质溶液中,如果有配体与蛋白质结合,则可检测到并测出结合产生的几百万分之一摄氏度的热量变化。
进行第一次注射时,微量热计测量被释放的所有热量,直到结合反应达到平衡,两个池的温度恢复到同一水平,信号也回到其起点。将第二小份配体试样注入到样品池中,同样微量热计测量被释放的所有热量。随着滴定的继续,配体与蛋白质之间的摩尔比随着一系列配体样品的注入而逐渐增加。蛋白质越来越饱和,配体结合的次数越来越少,并且热量变化开始减小,直到样品池中的配体数量相对于蛋白质而言最终表现出过量为止,从而使反应朝饱和的方向进行。
三、结果和数据分析对每个峰的面积进行积分,并以配体与蛋白质的摩尔比作为横坐标进行绘图。由此得出的等温线可拟合至导出亲和力(KD)的结合模型。结合等温线中心的摩尔比即为反应化学计量。下图给出了1:1结合反应的示例图。
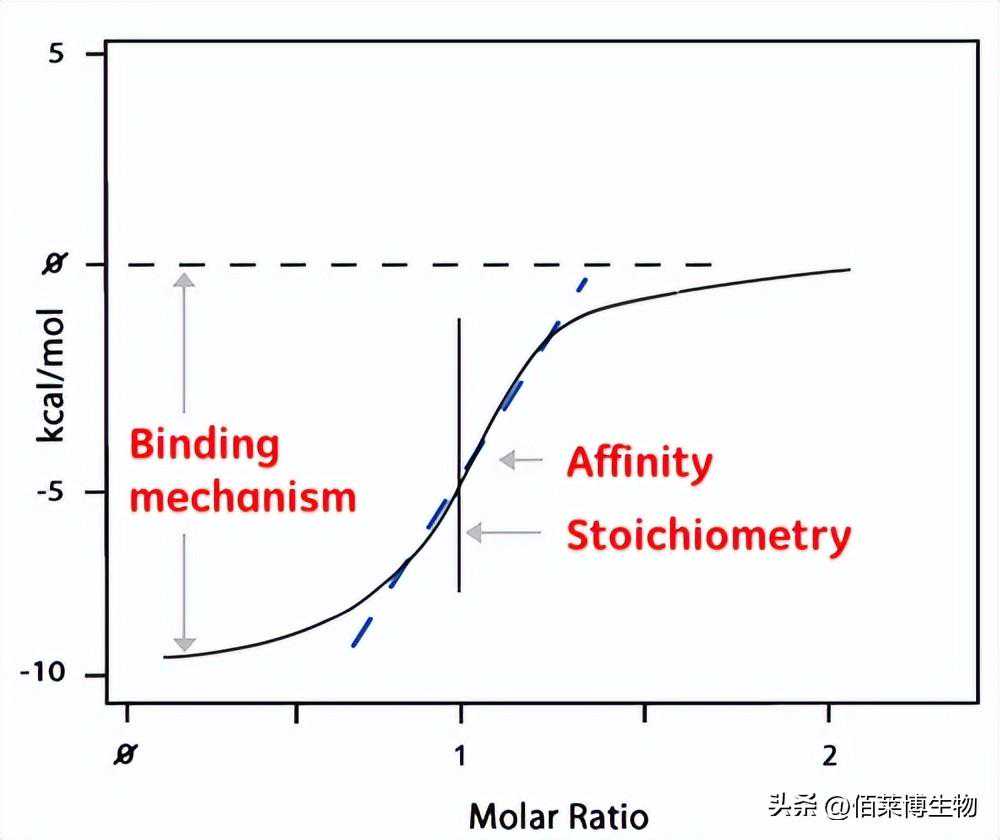
焓(ΔH)也可通过等温线直接导出,它表示每摩尔结合配体所释放的热量。这就意味着一次ITC实验就可提供丰富的结合反应信息,有助于理解相互作用的性质并探索热力学驱动因素。









