(报告出品方/作者:华安证券,王强峰,刘天文)
1、层析介质:生物制药分离纯化核心材料,预计2025年国内市场空间超过100亿1.1、色谱分离/层析是生物制药行业关键步骤
生物药与化学药生产方式区别大,生物药对纯化技术要求更高。药品按照制备方式的不同可以分为化学药和生物药,化学药是指化学合成的药品,一般是小分子药物。而生物药是指通过细胞、生物体或者发酵等方式合成的药品,一般是大分子药物。由于两者的生产方式之间的差距,导致了其后续纯化方法和纯化难度差距较大。化学药采取的纯化方式主要是过滤、萃取等传统工艺,而生物药则需要采用色谱分离/层析的方式来对产品进行分离纯化,其纯化难度远高于化学药。此外,为了达到更好的分离纯化效果,层析往往需要进行多次。一般而言,纯化按照CIPP纯化三部曲进行,即:捕获(capture)→中度纯化(intermediatepurification)→精细纯化(polish)。
色谱分离/层析是生物制药行业分离纯化的关键技术,其核心在于色谱填料/层析介质。色谱/层析技术是生物制药行业分离纯化的关键技术。其原理是利用混合组分中各个成分物质的物理和化学性质差异,与色谱填料作用力不同,使得各组分物质在层析柱的迁移速度有差异最终各组分按顺序从层析柱另外一端流出从而实现各组分的分离。色谱分离/层析技术的核心是色谱填料/层析介质,色谱柱的分离纯化效果及分析检测性能很大程度上取决于层析介质的形貌、结构、粒径大小和分布、孔径大小和分布、材质组成及表面功能基团等。
层析介质是色谱分离技术核心材料,不同层析介质工作原理不同,下游应用领域差异较大,因此选择标准也灵活多样,主要可分为以下两种:层析介质选择标准一:根据目标蛋白和杂质分子量的大小选择。色谱分离按照所分离物质分子量的大小可以分为中小分子分离纯化和大分子分离纯化,中小分子分离纯化通常要选择亲水层析介质、正相层析介质和反向层析介质,大分子分离纯化通常要选择亲和层析介质、离子交换层析介质、疏水层析介质和体积排阻层析介质。其中,亲和层析介质和离子交换层析介质是在大分子分离纯化中使用最多的层析介质材料。
1.2、需求端:生物制药行业快速发展,层析介质迎黄金时期
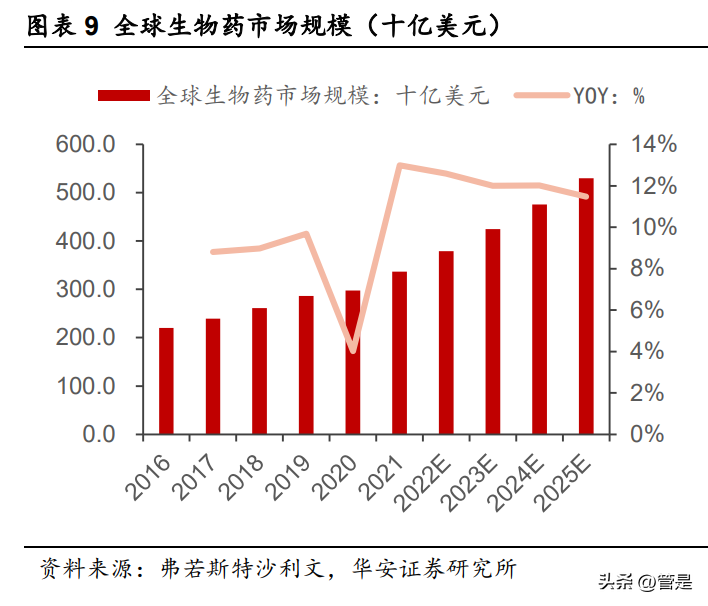
全球生物药进入快速发展时期,2020-2025年复合增速达12.20%。根据弗若斯特沙利文的统计数据,2020年全球生物药市场规模为2979亿美元,预计到2025年将增长至5301亿美元,2020-2025年复合增速达12.20%,远超同期化学药的5年复合增速2.80%。而且,从全球药物市场占比的角度来看,2021年全球生物药市场份额为24%,2025将提升至32%,增速显著。未来,全球生物药将持续保持快速发展的态势,这将拉动上游材料需求的快速增长。
全球在研生物药基数大且快速增长,为生物药市场持续发展奠定基础。根据CMP数据库的统计数据,2021年全球在研生物药数量为770个,其中三期临床项目156个,2016-2021年复合增速达28.23%。二期临床项目由2016年的42个上升至2021年的307个,2016-2021年复合增速达48.86%。一期临床项目也从11个增长至307个,2016-2021年复合增速达到了189.05%。全球在研生物药基数大且呈现快速增长态势,后续随着项目的不断落地,全球生物药市场有望持续高速发展。
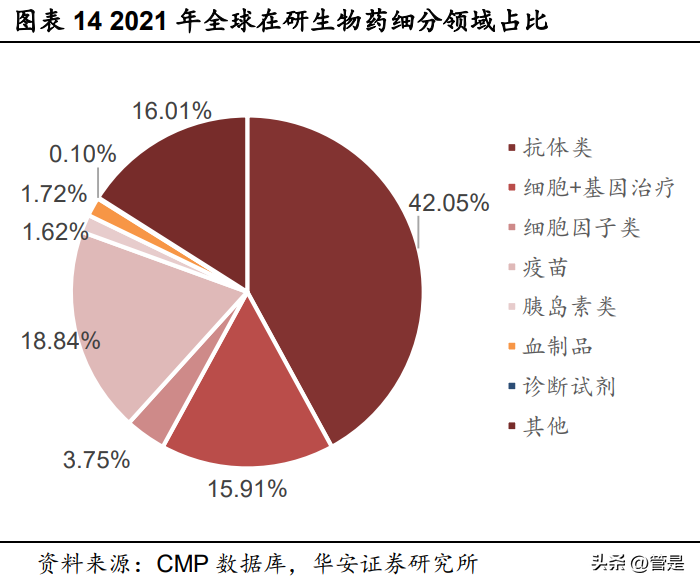
从全球在研项目细分领域来看,抗体类项目遥遥领先。根据CMP数据库的统计数据,2021年全球在研的987个生物药项目中,抗体类药物达到415个,占比为42.05%。其次为疫苗和细胞/基因治疗类药物,分别为186和157个,占比分别为18.84%和15.91%。预计后续抗体类药物将成为拉动生物药发展的主要动力,疫苗紧随其后,细胞/基因治疗类药物也将随着技术的不断进步逐步开启大规模商业化之路。
中国生物药市场规模增速远超全球。根据弗若斯特沙利文的统计数据,2020年中国生物药市场规模为3457亿元,预计到2025年将增长至8116亿元,2020-2025年复合增速达18.61%,超过同期全球增速6.41pcts,这表明中国生物药市场正在持续追赶,未来有望达到全球领先水平。
从新药IND和获批上市的角度来看,我国生物药占比稳定增长。根据医药魔方的统计数据,2021年我国新药IND数量为644个,而2016年才125个,5年年复合增速达到了39.65%。从新药IND的结构来看,2016年生物药占比为22.40%,2021年该比例提升至了35.40%。同时,从新药获批的角度来看,2016年我国仅获批新药7个,2021年该数据提升至65个,5年年复合增速达到了56.16%。虽然生物药的比例有所降低,但是绝对数额提升显著,而且,自2017年开始,我国生物药在获批新药中的占比基本呈现稳定增长态势。
从中国CDE注册申报和NMPA批准上市的生物药来看,抗体类项目也是遥遥领先。根据CMP数据库的统计数据,2021年我国CDE注册申报的生物药项目中,抗体类药品以52%的占比遥遥领先,其次为疫苗,占比为10%。2021年中国NMPA批准上市的生物药项目中,抗体类以30%的占比居于首位,其次为胰岛素和疫苗,占比分别为26%和16%。我国生物药的发展趋势和全球基本保持一致,呈现以抗体和疫苗为主导,其余各类方向互相补充的发展格局。
1.2.1、抗体:中国市场增速远超全球,在研项目丰富发展持续性可期
中国抗体加速追赶国际市场,全球市场份额快速提升。根据弗若斯特沙利文的统计数据,2020年全球抗体市场规模为1744亿美元,而同期我国抗体市场规模仅为411亿元,我国抗体全球市场份额占比约为3.4%。而根据沙利文的预测,到2025年,我国抗体市场规模将达到1945亿元,全球市场份额占比也将快速提升至9.5%。而且,我国抗体市场在2025年之前都能维持在20%以上的市场增速,也是远超同期全球市场增速,这说明我国抗体正在加速追赶国际市场,增长持续性强。
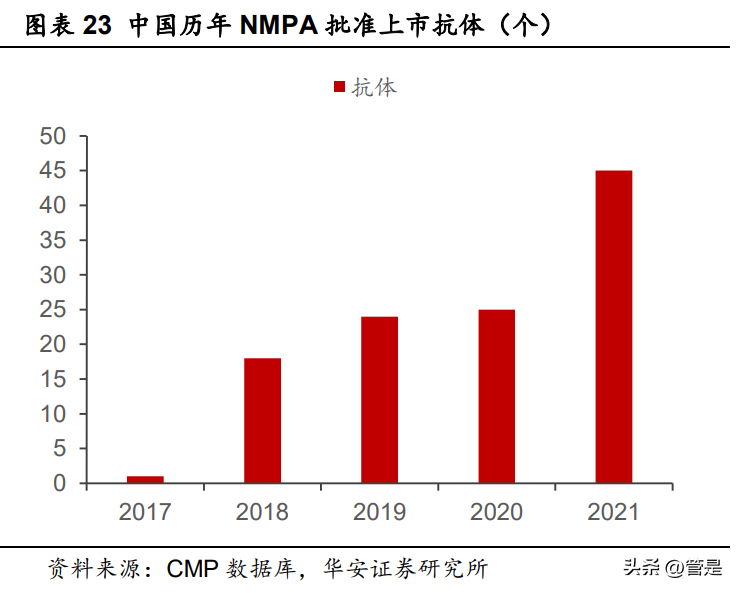
我国抗体CDE注册申报和NMPA批准上市数量稳步增长。根据CMP数据库的统计数据,2017年我国抗体CDE注册申报和NMPA批准上市数量分别为202个和1个,2021年,两者分别上升至1037和45个,增速显著。这意味着我国抗体市场逐步进入到快速发展时期,注册申报个数的增加也为后续项目落地奠定基础。
我国抗体产能加速释放,包括层析介质在内的耗材需求旺盛。由于抗体行业的快速发展,市场需求开始扩大,我国企业也在加大力度布局。据不完全统计,我国主流企业现有抗体产能32.5万升,在建产能33.6万升,规划待建产能25万升,在建产能+规划产能远超现有产能。随着新增抗体项目的不断落地,将快速拉动包括层析介质在内的耗材增量需求。而且由于层析介质需要定期更换,存量需求也会随着产能的增加而增长,抗体用耗材需求处于快速增长期。
1.2.2、疫苗:国内企业加速布局,新冠常态化加速国产疫苗需求
全球疫苗市场规模持续增长。根据弗若斯特沙利文的数据,2016-2020年间,全球疫苗市场规模从275亿美元增加至365亿美元,复合增长率为7.33%。在创新疫苗陆续上市、全球经济不断发展及中国、印度和俄罗斯等新兴市场的需求增长等因素推动下,未来全球疫苗市场规模将进一步扩大,预计在2025年将达到809亿美元。相应地,2020-2025年间,全球疫苗市场规模复合增长率达17.25%。
从细分市场来看,由于当前欧美疫苗市场既有品种接种率已经达到较高水平,因此未来增长空间相对有限。而以中国、印度等为代表的新兴市场新型疫苗供应不足且接种率较低,而且中国是增长的重要推动力量。在新冠常态化的背景下将加速疫苗需求,因此在未来5-10年内将成为全球疫苗市场规模增长的重要推动力量。根据弗若斯特沙利文的数据,我国疫苗市场规模在2020年为753亿元,预计到2025年将增长至2065亿元,复合增长率达22.36%,远超全球增长水平。
我国疫苗CDE注册申报数量稳步增长,NMPA批准上市疫苗近两年创新高。根据CMP数据库的统计数据,2016年我国抗体CDE注册申报和NMPA批准上市数量分别为20个和5个,2021年,两者分别上升至200和23个,增速显著。而且,从批准上市疫苗的角度来看,2020年和2021年的数量明显高于前几年,主要为新冠疫情影响下对疫苗的需求快速提升。而且,后续新冠将长期与人类共存,或进一步推升相关疫苗的需求。
从产能端来看,我国疫苗产能和品类丰富性显著提高。由于政府利好支持政策和免疫规划疫苗品种扩容等,叠加短期新冠疫情的刺激,中国免疫规划疫苗增长迅速。同时,长期来看,考虑到居民支付能力和支付意愿随人均可支配收入的增加而提升,民众疫苗接种意识不断增强及新型疫苗的推出和可及性改善,未来几年非免疫规划疫苗市场规模也将持续上升并持续占据主导地位。疫苗的可持续性需求刺激我国企业加大布局力度,产品种类也日益丰富,这将拉动疫苗用耗材的需求增长。
1.2.3、重组蛋白:市场规模不断扩大,进口替代稳步推进
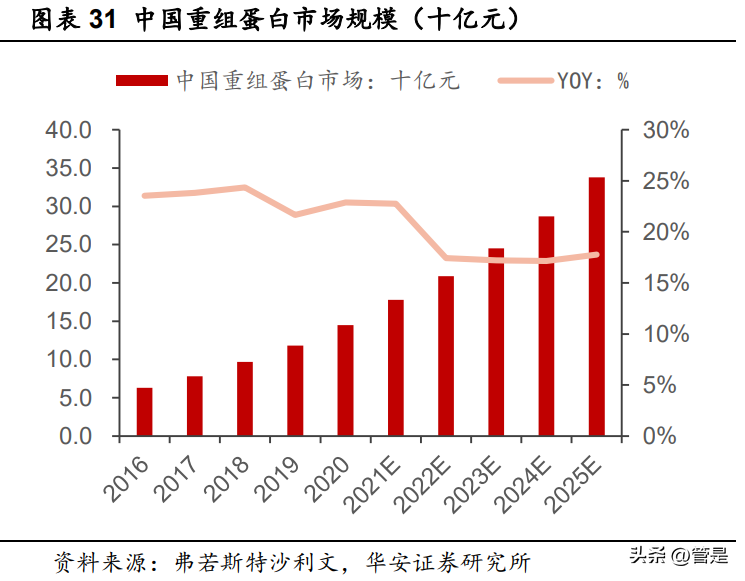
全球重组蛋白市场规模不断扩大。根据弗若斯特沙利文关于全球重组蛋白市场规模分析及预测,全球重组蛋白市场从2015年的70亿美元增长到2020年的108亿美元,期间年复合增长率为9.0%,预计2025年市场规模将达到208亿美元,2020年至2025年间年复合增长率接近14.1%。从国内市场来看,随着国内生物制药行业的蓬勃发展以及新冠疫情的影响,重组蛋白市场发展势头强劲。根据弗若斯特沙利文关于国内重组蛋白的市场规模分析及预测,国内重组蛋白市场规模从2015年的51亿人民币增长到2020年的145.4亿人民币,期间年复合增长率为23.3%,预计2025年市场规模将达到337.7亿人民币,2020年至2025年间年复合增长率接近18.4%,增速也是远超同期全球市场。
我国重组蛋白申请数量中国产项目显著增加。根据火石创造统计的数据,2021年我国共受理重组蛋白申请414个,其中国产231个,进口183个,国产重组蛋白受理数量超过了进口重组蛋白。从细分领域来看,包括IND申请80件、补充申请16件、仿制药补充申请224件、申请生产销售45件及其他申请49件。未来,随着申请项目的不断推进和正式落地,我国国产重组蛋白行业有望加速发展,将通过价格、供应链及服务的优势提升市场竞争力,逐步打破进口产品主导的行业局面,形成进口替代发展趋势。
国内企业不断实现技术突破,产能加速释放抢占市场份额。以国产重组蛋白企业近岸蛋白为例,其现有重组蛋白产能6.48万升,产品结构丰富,包括靶点及因子类蛋白、重组抗体、酶及各类试剂。同时,公司能够根据各产品下游市场的需求变化情况,及时调整并优化产品结构,始终保持各装置产能高效利用。我们预计,随着国内企业不断实现技术突破,优化产品成本和结构,国产重组蛋白产能有望加速释放,进一步抢占市场份额,稳固进口替代发展趋势。
1.2.4、细胞及基因治疗:新技术逐步进入释放期,我国企业进展顺利
细胞治疗新赛道快速发展,市场规模飞速增长。自2017年全球首批两个CAR-T产品获批以来,全球CAR-T细胞治疗迅速发展。根据弗若斯特沙利文关于全球CAR-T细胞治疗市场规模分析及预测,2021年全球CAR-T细胞治疗市场规模约19亿美元,预计到2025年将提升至90亿美元,2021年至2025年间年复合增长率达到47.53%。从国内市场来看,我国细胞治疗起步虽然略晚于国外,但是从2021年开始,我国细胞治疗逐渐追赶国外市场,步入快速发展阶段。根据弗若斯特沙利文的统计数据,2021年我国CAR-T细胞治疗市场规模仅2亿元,但到2025年将提升至80亿元,2021年至2025年复合增长率达到151.49%,远超同期全球水平。
基因疗法作为新一代精准医疗方法,正在快速兴起。近年来,在基础生命科学和前沿生物科技进步的推动下,以基因疗法为代表的新一代精准医疗快速兴起,发展趋势明晰,对以小分子和大分子药物为主的创新药市场起到了重要的补充、迭代和开拓作用。根据弗若斯特沙利文关于全球基因治疗市场规模分析及预测,2016年全球基因治疗市场规模约5040万美元,2020年提升至20.8亿美元,2016年至2020年间年复合增长率达到153.46%。预计到2025年,全球基因治疗市场规模将达到近305.4亿美元,2020年至2025年间年复合增长率达到71.20%。
从注册申报和批准上市产品来看,国内细胞治疗和基因治疗渐入佳境。根据CMP数据库的统计数据,2021年CDE共受理细胞和基因治疗产品59个,是近六年新高。其中IND申请52个、补充申请3个及仿制药补充申请4个,产品涉及免疫细胞类、干细胞类、病毒类和基因治疗类。从获批上市产品来看,目前还主要是细胞治疗,基因治疗尚处于研究和发展阶段,未来有望实现产品的上市销售。从产能端来看,我国企业正处于起步阶段,未来空间极大。根据各公司披露的公开数据,目前各公司的产能大多处于千升级别,主要是目前行业处于起步阶段,下游需求还未完全释放。未来随着行业不断发展,技术不断进步,细胞治疗和基因治疗需求有望快速起量。
1.3、国内生物药产能飞速扩张,2025年我国抗体用层析介质市场规模有望超百亿元
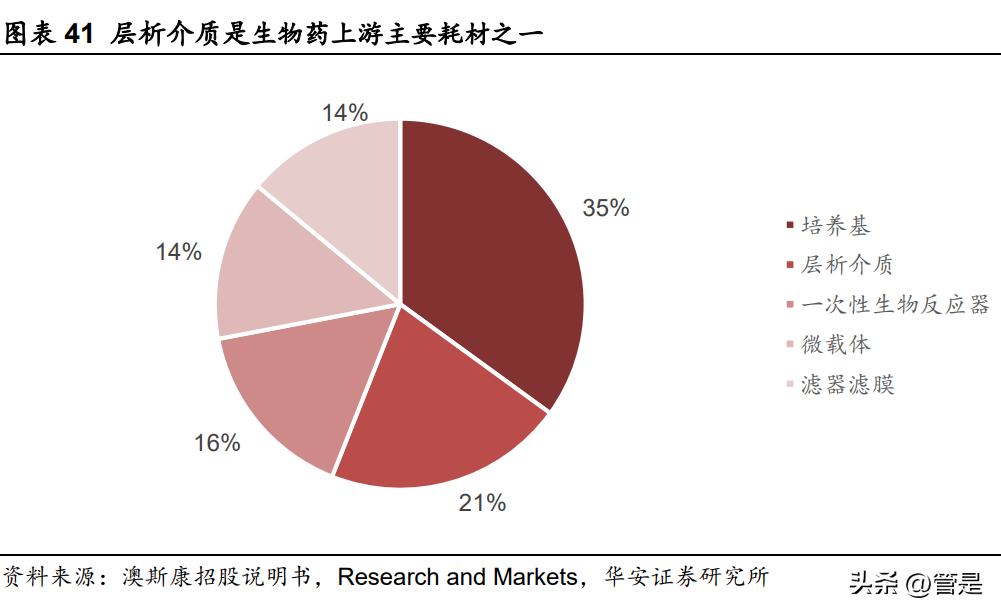
层析介质是生物药上游主要耗材之一,占原材料成本的21%。生物制药产业依靠细胞体外培养工艺实现各类大分子生物药的体外大规模生产,该过程中通常会产生各类不同的成分,而层析介质是分离出有效成分最关键和必不可少的原材料。根据澳斯康招股说明书援引ResearchandMarkets的分析,层析介质是生物制药上游原材料、耗材品种中市场规模第二大品类,其总体市场规模占比达到21%,仅次于培养基。
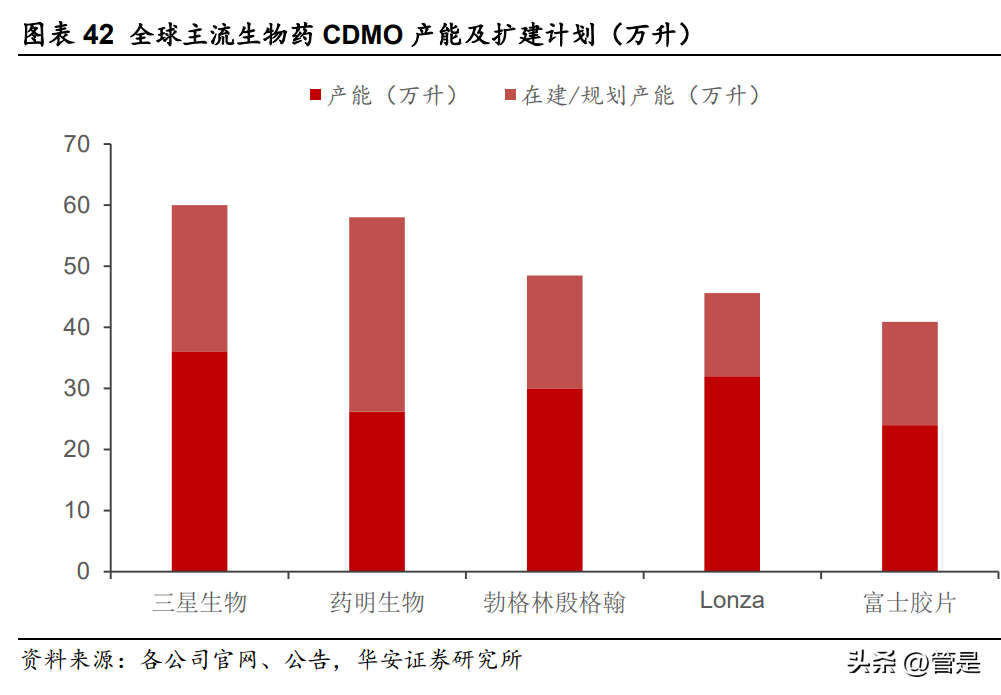
全球主流生物药CDMO产能快速扩张,预计2025年将达到253万升。根据各公司披露的现有产能及扩产公告,全球五大主流的生物药CDMO企业合计拥有产能148.2万升,其中三星生物产能36万升,位居全球第一,其次为Lonza和勃林格殷格翰,分别拥有产能32万升和30万升。中国生物药CDMO企业龙头药明生物拥有产能26.2万升,位居全球第四。从新增产能来看,三星生物、勃林格殷格翰、Lonza、药明生物和富士胶片分别预计新增24万升、18.5万升、13.6万升、31.8万升和16.9万升,产能增速分别为66.67%、61.67%、42.50%、121.37%和70.42%,整体呈现快速增长态势。
其中,药明生物以121.37%的产能增速位居第一,扩产完成后,药明生物总产能将达到58万升,仅次于三星生物。同时,其他国产生物药CDMO企业产能也在不断新增,我国生物药全球产能占比进一步提升,这将拉动国产层析介质需求快速增长。
2021年我国层析介质市场规模约66亿元,预计2025年将达115亿元。根据BioPlan的统计数据,2018年全球生物药产能合计约1650万升,至2021年,该产能提升至1738万升。其中,中国的生物药产能从2018年的86万升提升至2021年的184.32万升,增速远超全球,预计该趋势还将进一步维持。根据上述统计数据,结合相关产品价格,我们估算得出,2021年我国层析介质市场规模约66亿元。同时,根据上述国内企业生物药产能扩张计划,预计未来3年我国抗体用层析介质市场规模有望达到15%以上年复合增速,则至2025年,我国抗体用层析介质市场规模将达到115亿元。
2、供给端:行业准入壁垒高,生物制药降本趋势下国产填料大有可为2.1、层析介质技术壁垒高,国外企业仍占据行业主导地位
国外企业具备先发优势,占据全球层析介质主导地位。根据纳微科技招股说明书的数据,2018年全球色谱填料行业基本被外国企业所占据,GE、Tosoh和Bio-Rad三家企业全球市占率分别为35%、8%和7%。从收入端来看,2021年GE和Agilent生命科学领域(注:由于两个企业未单独披露层析介质收入,以生命科学领域代替)分别为150亿美元和28.23亿美元,远超国内企业如纳微科技和蓝晓科技,国产企业在层析介质领域任重而道远。层析介质作为色谱分离技术核心材料,其制备难度极高,叠加下游客户验证过程繁琐且周期较长,因此行业准入壁垒高。
层析介质行业壁垒之一:制造壁垒。层析介质通常是指具有纳米孔道结构的微球材料,其粒径在微米尺度范围内,而层析介质上的孔径则以纳米衡量,常规孔径大小在5-200纳米范围内。从组成和结构上来看,影响层析介质性能的两大因素为基体材料和官能团。基体材料主要通过材料的种类、粒径大小和粒径分布、孔径大小和孔径分布来影响层析介质的载量、反压等指标;官能团则主要通过改变其功能基团性能和密度来影响纯化的模式和效果。也正是因为影响层析介质性能的参数众多,且控制不同参数的难度较大,因此层析介质生产难度极大。
层析介质行业壁垒之二:品类壁垒。层析介质种类多样,按照基质材料的不同可以分为无机材料和有机材料,无机材料主要用于中、小分子分离纯化中,有机材料主要用于大分子分离纯化中。从分离机理来看,层析介质又可以分为亲和、离子交换、疏水、体积排阻等类型,各类型又可以根据孔径、官能团的密集程度等继续细分。因此,层析介质行业的另一壁垒主要来自于其丰富的品类。而且下游客户往往会对层析介质制造企业提出配套生产的要求,进一步提高了行业的准入壁垒。
层析介质行业壁垒之三:客户壁垒。层析介质作为生物药大分子分离纯化核心材料,其下游客户主要为医药企业。而医药企业的特性决定了其较长的产品验证周期,一般一款层析介质需要半年到三年不等的验证时间,过程较为繁琐。同时,尤其医药企业在申请新项目时需要提交申请流程,其中层析介质也在审核之列,一旦更换新的层析介质需要重新审核,因此下游客户在选择了一款产品之后短期难以更换,进一步增加了客户黏性,提高了行业准入壁垒。
2.2、下游降本+政策支持+企业技术突破,填料国产替代加速
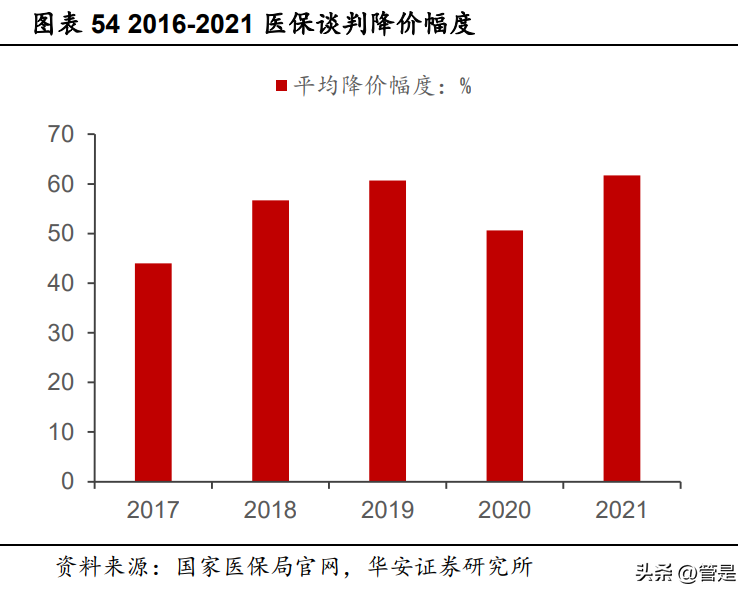
集采和医保谈判政策下药品价格降幅较大,行业降本动力足。在老龄化的压力下,我国医保的支付压力较大。因此,在集采政策的推动下,我国相关药品价格出现出较大幅度下降。目前,集采已经来到了第七批,此次药品价格平均降幅为48%,一次竞争激烈的药品甚至降幅超过了90%。同时,考虑到医保在国内的强势地位,近几年医保谈判的药品均有较大降价幅度。在下游药企产品价格稳步下降的趋势下,其降本动力也是日益充足,层析介质作为其核心原材料之一,亦在降本之列。而目前国内药企大多采用进口层析介质,其价格远高于同品类国产层析介质,在降本的趋势下国产层析介质有望加速替代进口产品。
我国政策支持医药材料自主化,国产层析介质发展空间广阔。我国政策持续保障新材料的发展环境,早在2017年,我国就曾印发《“十三五”材料领域科技创新专项规划》的通知国科发高〔2017〕92号文件,提出要重点发展基础材料技术提升与产业升级、战略性先进电子材料、材料基因工程关键技术与支撑平台、纳米材料与器件、先进结构与复合材料、新型功能与智能材料、材料人才队伍建设。2021年,《中华人民共和国国民经济和社会发展第十四个五年规划和2035年远景目标纲要》指出要加强医用材料研发应用,而层析介质作为一种“卡脖子”材料,必须实现国产化。在我国政策的持续支持下,国产层析介质发展空间广阔。
我国企业逐步实现技术突破,部分产品性能已经达到国际领先水平。在我国政策的大力支持以及下游药企不断增强的国产替代动力下,我国层析介质相关企业也在加大研发力度,产品品类和性能不断提升,部分产品相关性能已经达到了国际领先水平。以ProteinA亲和层析介质为例,目前全球市场以GE为主。由于亲和层析介质是层析中用量最大的品类之一,而且较高的技术壁垒赋予更高的单位价值,因此亲和层析介质是国产替代的重点品种。目前,国内企业如纳微科技、博格隆、蓝晓科技等企业均推出了各自的ProteinA亲和层析介质,以蓝晓科技为例,公司产品在耐压、动态载量和配基密度等方面已经能够做到与GE持平甚至是小幅超越,体现了国产层析介质较强的产品竞争力。
国产层析介质产能加速释放中。在国内政策的不断支持下,我国层析介质企业不断加大研发投入,在部分产品上逐渐实现技术突破,并开始进入下游企业供应链中。从产能方面看,目前纳微科技拥有产能12.28万升,赛芬科技拥有产能10万升,博博隆拥有产能8万升,蓝晓科技拥有产能7万升,随着我国企业产能的不断释放,层析介质有望加快国产替代进程。
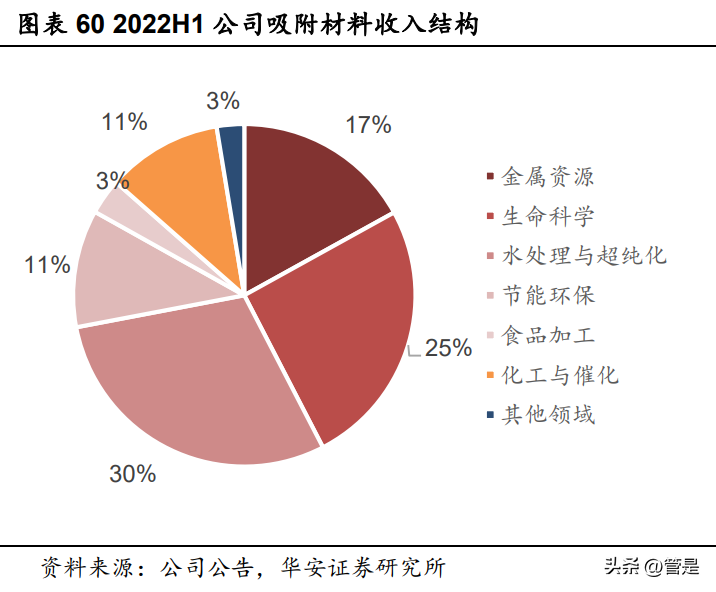
层析介质市场空间广阔,公司强化技术布局抢占市场空间。公司以吸附分离材料为基础,不断加大研发投入,扩充产品应用方向。目前,公司吸附分离材料已经广泛应用于盐湖提锂、化工催化、水处理等领域,弥补了国内部分高端吸附材料的空白。在公司长期的研发投入下,成功突破了均粒技术,产品一致性大幅提升,产品结构也逐步向层析介质等医用材料延伸。根据前文的测算,在2025年我国层析介质市场有望超百亿元,空间广阔。而且,目前大部分的市场还是被国外企业所占据,国产替代空间更大。而层析介质行业具备一定的技术壁垒,部分产品依旧有待实现技术突破。公司目前也在不断强化自身技术布局,相关产品专利数量不断增长,喷射法均粒技术的突破更是直接使得产品批量稳定性和综合性能得到了质的飞越,助力公司产品抢占市场份额。
得益于技术储备的增加,公司产品结构日益丰富。公司目前已经基本实现了硬胶和软胶的全面覆盖,可为客户提供包括亲和、离子交换等各类层析介质以及相关的后续服务,逐步受到客户认可,2022年公司生命科学领域的高速增长更是直接证明了公司相关产品处于快速放量期。新产品方面,公司第二代高耐碱性ProteinA亲和填料已完成多家客户抗体项目小试验证,综合性能获得客户的认可。mRNA纯化亲和填料oligodT及超大孔离子交换填料持续开发,完成部分客户测试,在载量、收率,纯度、短链RNA和环状RNA去除方面,具有较好效果。
oligodT亲和填料和超大孔离子交换填料开发成功,将极大的加速公司在mRNA领域产业化应用,提升市场竞争力。连续流层析系统开发方面,已经与客户合作完成工艺参数设计,并开始进行生产。随着公司多项技术的成功研发和落地,我们预计,未来生命科学领域将成为拉动公司业绩的新增长极。
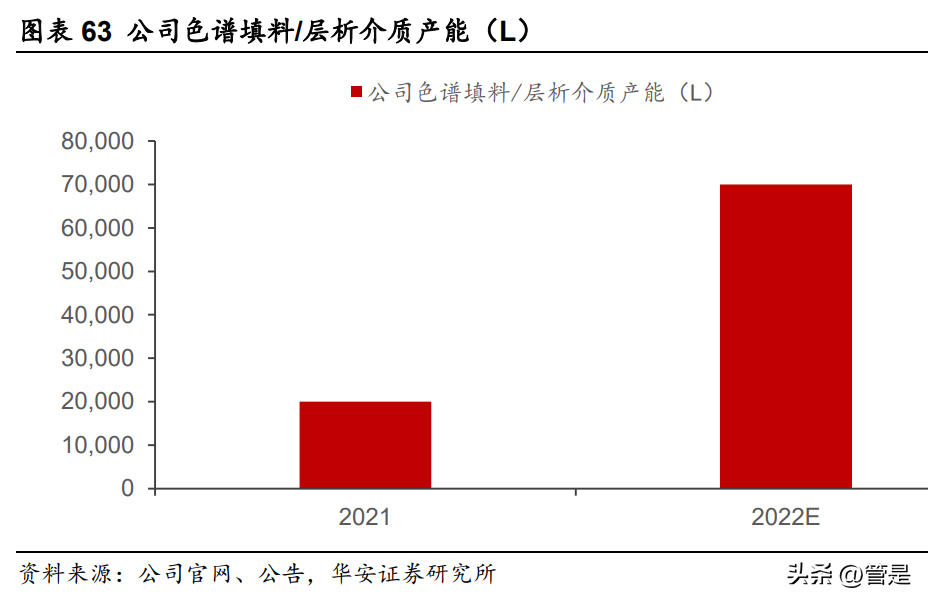
产能方面,公司新增50000L层析介质,2023将逐步释放。得益于前期的研发投入,公司目前已实现软胶和硬胶生产的全覆盖,此外,公司2022年新建50000升/年的层析介质生产线,总产能达到了70000升/年。新产能的建成,一方面将有效缓解现有产能不足,缩短供货周期,提升供应能力;另一方面,新生产车间参照GMP规范设计和建设,确保产品质量稳定。此外,新产能建成后,可实现单批次产量2000L,满足部分客户对填料单批次使用量的需求,提高客户自身产品的批次稳定性。
以层析介质为基,固相合成载体等产品陆续放量,生命科学大板块协同发展。从公司整体战略布局的角度来看,层析介质是公司生命科学大板块中的一员,其余的还包括如固定化酶、合成载体等产品。由于生命科学板块各个产品客户具备一定的重合,当某一种产品成功进入下游客户的供应链之后,客户可能会倾向于优先考虑同一公司的另一产品,因此公司生命科学多产品的布局有利于发挥整体的协同互补优势,促进各细分领域共同进步。而且,公司也在加大相关产品的研发力度,固定化酶载体突破7-ACA酶法工艺产业化,有效降低了传统化学法生产带来的环境污染问题,降低了企业的生产成本,促进了产业升级。
下游应用方面,公司固相化酶和合成载体多应用于现代常见病治疗药物的合成,比如公司多肽固相合成载体广泛用于多肽类和蛋白质合成领域,如心血管疾病药物、糖尿病药物、抗肿瘤药物等药物的合成与制备,拥有丰富的产品品系。而公司的Oligonucleotide固相合成载体则主要应用于核酸类药物的合成。此外,公司是全球多肽固相合成载体核心生产企业与主要提供商,相关产品在国内外知名药企与多肽CDMO企业中已规模化使用。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)









