
蛋白酶体抑制剂
蛋白酶体抑制剂(PI)是多发性骨髓瘤(MM)治疗的关键,无论是NCCN指南、MayoClinic指南还是我们中国的治疗共识,都将蛋白酶体抑制剂作为多发性骨髓瘤治疗的基石性药物(无论标危或高危)。
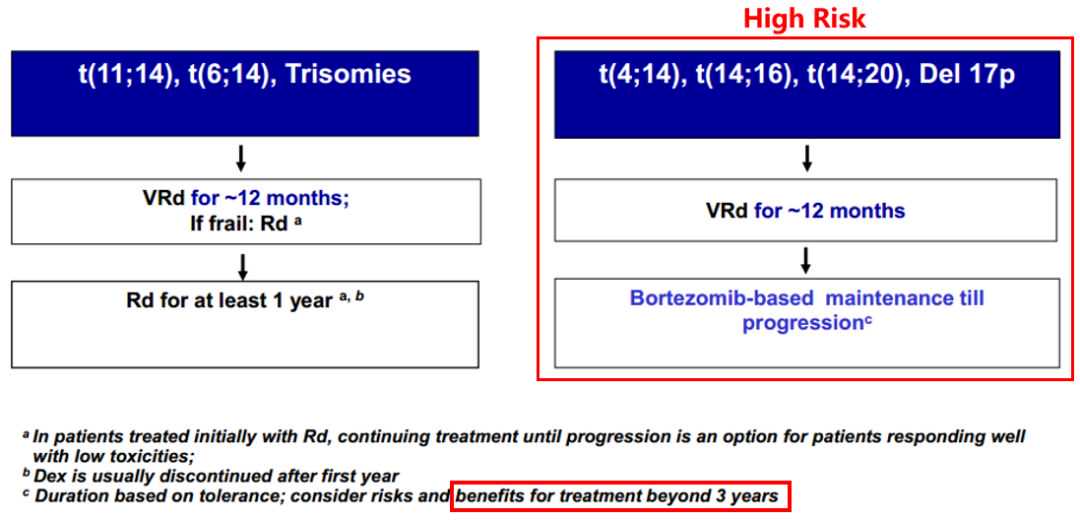
目前可用的蛋白酶体抑制剂主要是硼替佐米,卡非佐米,以及伊沙佐米,那这三种蛋白酶体究竟哪一种效果更好呢?遗憾的是目前并没有头对头的临床研究,最近知名化学生物杂志"CellChemicalBiology"对目前可用PI进行了体外实验,尝试从另一个角度来一次头对头的碰撞,让我们针对我国现有的蛋白酶体抑制剂来看看结果。
关于蛋白酶体
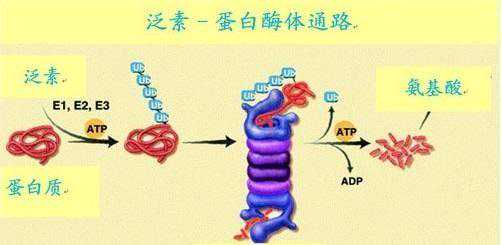
泛素-蛋白酶体系统是一种广泛存在于真核细胞内的依赖ATP的蛋白质降解体系。具有清除大多数短寿蛋白、错误折叠或损害蛋白,也包括部分长寿蛋白,起到调控蛋白质,维持细胞内环境稳定的作用,在细胞周期调控、信号转导、细胞凋亡、蛋白质的翻译转录及免疫应答等生命活动中发挥重要的作用。
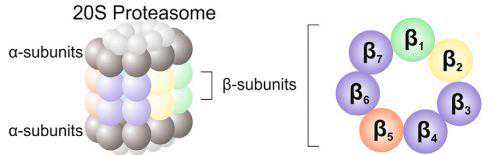
标准蛋白酶体(constitutiveproteasome)是26S蛋白酶体由催化核心20S蛋白酶体和2个19S的帽子组成,20S蛋白酶体是由2条外环α链和2条内环β链相互堆积形成的桶状结构,每条链分别由7个α亚单位和β亚单位组成。外环无催化活性,内环是催化中心所在的位置,20S蛋白酶体对底物作用的特异性取决于β1、β2、β5亚单位N2末端苏氨酸(Thr)残基上肽键。
免疫蛋白酶体(immunoproteasome)是20S蛋白酶体结构在IFN-γ、TNF、氧化应激、炎症反应或一氧化氮等刺激诱导下,其β亚单位的β1、β2、β5可相应被LMP2(β1i)、MECL-1(β2i)和LMP7(B5i)取代,组装成新的20S蛋白酶体,新蛋白酶体中LMP2和LMP7能够增强蛋白酶体产生与主要组织相容性抗原(MHC-1)相结合多肽的能力。
蛋白酶体抑制剂的抑制能力比较
研究意义
蛋白酶体的β5亚基最初被鉴定为蛋白酶体蛋白质转换的限速蛋白酶,因此之前所有设计的PI均靶点为标准蛋白酶体或免疫蛋白酶体的β5亚基。而后的研究发现,硼替佐米和卡非佐米除了抑制β5亚基外,还分别存在β1及β2亚基的共抑制,并使得MM细胞对硼替佐米和卡非佐米更为敏感(Mirabellaetal.,2011;Krausetal.,2015)。2016年,新的化学工具可以选择性操作和监测每个蛋白水解亚基的活性(deBruinetal.,2016).在化学工具的帮助下,很明显所有β5靶向的PI实际上在较高浓度下失去其仅针对β5亚基选择性,将同时共同抑制β1或β2型蛋白酶体亚基。这些共抑制模式在各个PI之间并不相同。
了解PI不同的共抑制模式可能有助于解释在头对头比较中使用不同PI或不同剂量的PI所观察到的令人困惑的差异:如卡非佐米是否优于硼替佐米在临床试验中出现了两种相反的结果(ENDEAVORvsCLARION,Dimopoulosetal.,2017a;Faconetal.,2017);又如每周一次高剂量的卡非佐米比每周两次的低剂量(ARROW试验)更具活性,且毒性并未增多(Moreauetal.,2018);又比如具有相似的累积剂量,而每周一次的硼替佐米剂量相较于每周两次的用药具有相似的活性,且副作用大大降低(Bringhenetal.,2010).
研究方法
1、这项研究中设计了一个类似于临床静脉给药()的药物动力学设置(1小时脉冲治疗),对测试的PI的抑制靶点及抑制力进行了头对头的比较。
2、为了直接解释功能蛋白酶体蛋白水解,研究配备了Ub-G76V-GFP的AMO-1细胞,量化了蛋白酶体底物蛋白在蛋白酶体抑制作用下的蓄积。Ub-G76V-GFP是一种泛素融合降解底物,通过功能抑制蛋白酶体蛋白水解途径,构建细胞内荧光信号(简单而言,MTS代表MM细胞存活率,UbGFP代表蛋白酶体抑制力,一般UbGFP越高,MM细胞死亡越多)。
3、对于β1、β2、β5亚基的活性情况,通过荧光化学探针ABP来显示。
抑制力结果
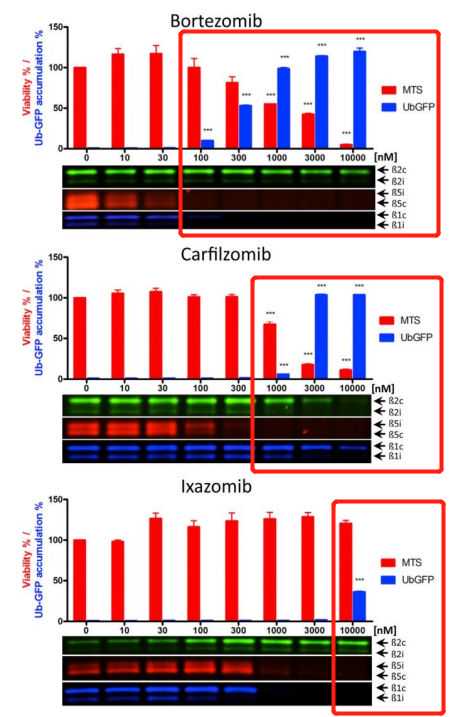
1、对于PI,单独抑制β5c/i亚基活性并不影响MM细胞活力的降解速率(如,BTZ30nM,CFZ300nM),这表明单独抑制β5c/i亚基活性对于MM细胞毒性是不够的。相反,只有当实现β5c/i5抑制并同时对至少一个另外的蛋白酶体亚基(β1或β2)共抑制时,才发生蛋白酶体水解的功能抑制。而当剂量增加后,所有PI都显示了对于β5c/i及β1或β2的共抑制,且UbGFP的荧光性明显增强,蛋白酶体水解功能被明显抑制,MTS比例大大降低,显示MM细胞毒性增强。
这个结果同时解释为何硼替佐米的药效学模型显示了一种剂量依赖的蛋白酶体抑制作用,这种抑制作用既与mg/m2的单剂量有关,也与提供的总剂量有关(Orlowskietal,2002)。
2、观察到硼替佐米在10nM浓度下已经实现了对β5c/i活性的50%抑制,而CFZ需要100nM,而伊沙佐米需要达到1,000nM,显示硼替佐米的抑制力最快显现。
3、硼替佐米累积剂量100~1000nm,从UbGFP的积累评估其蛋白酶体抑制力(UbGFP比例上升)和细胞毒性(MTS比例下降)是通过β5/β1联合抑制实现的(不影响β2活性),而卡非佐米累积剂量300~3000nm通过β5/β2联合抑制实现的蛋白酶体抑制和细胞毒性(不影响β1活性)。而伊沙佐米在脉冲暴露期间的靶上活性最弱,伊沙佐米对β5/β1的共抑制作用需要剂量在1000nm以上,仅在10000nm处对蛋白酶体蛋白水解的功能抑制较弱(UbGFP比例上升有限),不足以转化为细胞毒性(MTS比例依然很高)。
蛋白酶体亚单位抑制的持续时间
研究意义
环氧酮类PI(卡非佐米)由于其不可逆蛋白酶体抑制剂的化学性质被认为与可逆的蛋白酶体抑制剂肽硼酸盐(硼替佐米,伊沙佐米)相比具有抑制时间更长的优势。然而仅仅只是一种推测,并没有在直接头对头的比较中得到解决。为了寻找答案,该研究直接比较脉冲治疗后各个药物对于β5c/i抑制的持续时间。
剂量选择
为了排除药物不同细胞毒性的影响,研究主要比较了在1小时脉冲治疗条件下导致选择性抑制β5c/i活性的药物浓度。从上面抑制力研究中可以看出:
硼替佐米——30nM;
卡非佐米——150nM;
伊沙佐米——1000nM
使用荧光化学探针ABP对β5c/i亚基状况进行了72小时的时间跟踪。
持续力结果

1、所有PIs在脉冲1小时后均表现出对β5c/i的完全抑制。
2、在24小时内,所有设置的细胞都恢复了蛋白酶体β5c/i活性至50%。
3、在持续抑制时间方面,三种药物并没有统计学差异。
选择性抑制β5/β2亚基能克服硼替佐米耐药
研究意义
硼替佐米作为骨髓瘤治疗的基石药物,在患者多次复发后不可避免的将会造成耐药,在这种情况下,是对β5c/i及β2c/i具有共抑制作用的药物能够克服耐药(如卡非佐米),还是具有相同β5c/i及β1c/i共抑制作用的药物依然能够有效(如伊沙佐米)?
研究方案
为研究共抑制β5c/i及β2c/i亚基是否能够克服硼替佐米的耐药性,使用了之前描述的硼替佐米/卡非佐米耐药细胞株AMO-1(Besseetal.,2018)、RPMI8226、L363cells(aBtz,aCfz),并结合体外48小时PIs连续治疗。观察不同的抑制组合是否能够最终克服耐药情况。
研究结果
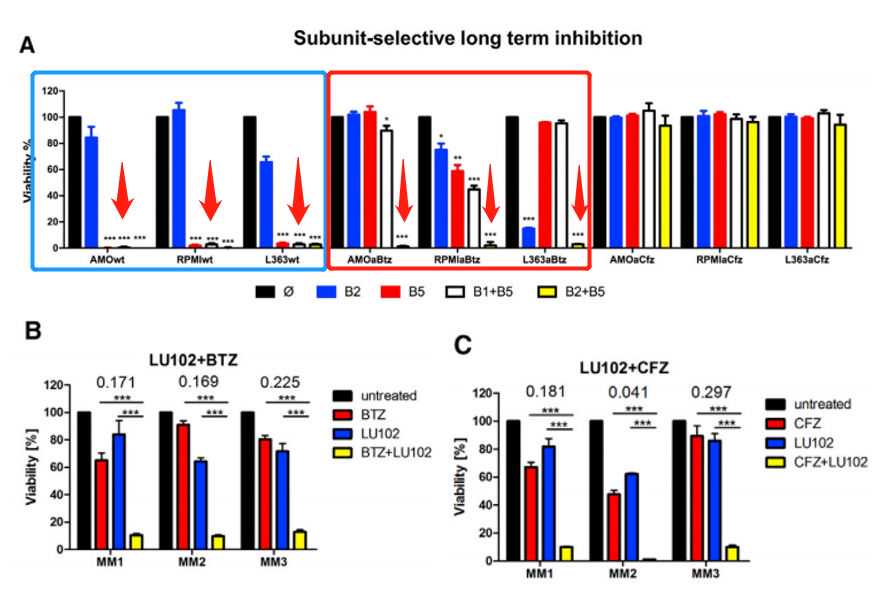
1、在PI敏感细胞(野生型)中,单独抑制β5c/i已经导致显著的细胞毒性,而选择性β2c/i抑制则无效。(蓝框中,野生型细胞株对于选择性抑制β5c/i亚基就非常有效,而若仅仅选择性抑制β2c/i亚基则无效)
2、硼替佐米耐药细胞对选择性β5c/i亚基抑制不敏感;对于同样β5c/i和β1c/i的协同抑制机制的用药并没有显示出非常好的疗效。然而,β5c/i和β2c/i的协同抑制可以克服抗药性(红框中,黄色β5c/i和β2c/i的协同抑制条显示有效,并同时显示出具有很强的协同细胞毒性)。但是对卡非佐米耐药细胞株则并无疗效。
3、同样,将硼替佐米(Btz)与β2c/i抑制剂LU-102联合应用,可以克服MM患者原发恶性浆细胞对BTZ的耐药性(B图)。同样,LU-102联合Cfz能够克服MM患者原发恶性浆细胞对Cfz的耐药性
总结
虽然本研究的头对头仅限在体外研究上,但是还是能够通过化学方法发现我们常用的三种蛋白酶体抑制剂的不同,需要我们记住以下知识点:
1、三种PI都能选择性抑制20S蛋白酶体上的β5亚基,当剂量累积上升时,会产生共抑制状态,这种状态有利于对MM细胞毒性的产生,其中硼替佐米/伊沙佐米为共抑制β5c/i和β1c/i亚基,卡非佐米共抑制β5c/i和β2c/i亚基。
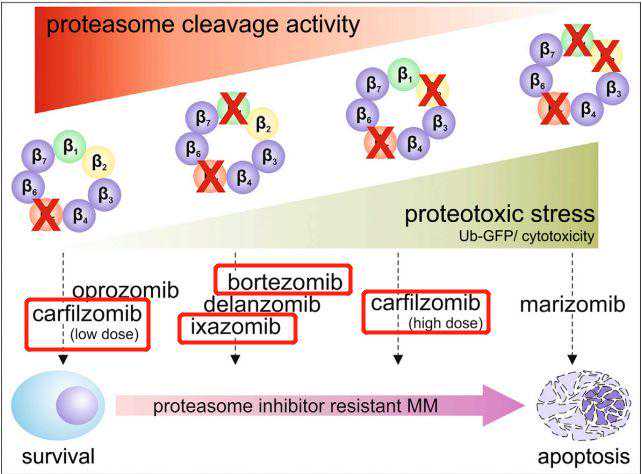
2、抑制力方面,硼替佐米体现了最强的抑制力,在10nM浓度下已经实现了对β5c/i活性的50%抑制,而CFZ需要100nM,而伊沙佐米需要达到1,000nM。此外对于共抑制达到对MM的细胞毒作用,硼替佐米和卡非佐米均显示出较好的疗效,而与此对比的是伊沙佐米需要大剂量(10000nm以上)显示出对蛋白酶体蛋白水解的功能较弱的抑制,且不足以转化为细胞毒性。
3、对蛋白酶体抑制的持续时间方面,三种药物并没有显示出统计学差异。
4、对于硼替佐米耐药的细胞株,应用β5c/i和β2c/i共抑制药物治疗能够体现出较好的疗效,而使用与硼替佐米相同机制的β5c/i和β1c/i共抑制药物并未在体外试验中展示出较好的疗效,提示我们对于硼替佐米耐药的患者卡非佐米是个不错的选择,而伊沙佐米未必有效。









